8 Mythen über Krankheitserreger-Tests

Mythos 1
Tests auf Umweltpathogene verbessern mein Lebensmittelsicherheitsprogramm nicht
Die meisten Vorschriften für Krankheitserreger verlangen eine Untersuchung des Endprodukts, bevor eine Charge der Lebensmittelproduktion sicher für den Vertrieb und den Einzelhandel freigegeben werden kann. Die Untersuchung von Endprodukten ist jedoch mit mehreren Herausforderungen verbunden. Erstens erschweren Variablen wie die Hintergrundmikroflora, hemmende Eigenschaften, der pH-Wert und die Salzkonzentration den Nachweis von Krankheitserregern. Zweitens können die Probenahmeverfahren und die Heterogenität der Proben zu Ungenauigkeiten führen, insbesondere wenn die Kontamination sehr gering ist. Wie können Lebensmittelhersteller sicher sein, dass die Anzahl der getesteten Proben ausreicht, um sicherzustellen, dass die Partie völlig frei von gefährlichen Krankheitserregern ist? Umwelttests haben sich in vielen Programmen zur Lebensmittelsicherheit als sehr nützliches Instrument erwiesen und wurden im Rahmen des FDA Food Safety Modernization Act (FSDA) als Teil der Präventivkontrollen angepasst. Umweltüberwachungsprogramme (oder EMPs) ermöglichen es einem Lebensmittelhersteller, Wachstumsnischen in Produktionsbereichen zu finden und Maßnahmen zu ergreifen, um jedes Risiko einer Lebensmittelkontamination zu beseitigen. Bereiche, in denen ein hohes Risiko einer Kontamination mit Krankheitserregern besteht, sollten beprobt werden, da der Zweck von Umwelttests darin besteht, positive Ergebnisse zu finden. Das Ziel der Überwachung ist es, potenzielle Krankheitserreger aus der Anlage und der Produktionslinie auszumerzen, bevor es zu einer tatsächlichen Kontamination kommt, und den Lebensmittelherstellern einen frühen Hinweis auf ein Kontaminationsrisiko/-problem zu geben.
Mythos 2
Interne Tests auf Krankheitserreger erfordern erhebliche Investitionen
Servicelabore sagen ihren Kunden oft, dass es zu teuer und zu aufwändig ist, in ihrer eigenen Einrichtung auf Lebensmittelpathogene zu testen. Das mag stimmen, wenn Standardverfahren (FDA BAM, ISO) verwendet werden, da diese in der Regel viel Zeit in der Praxis erfordern. Andere Methoden wie ELISA und Echtzeit-PCR erfordern eine teure Ausrüstung. In der Tat sind die einzigen Geräte, die Sie für Inhouse-Tests benötigen, ein Inkubator für die Anreicherungsphase und eine Waage zum Wiegen der Proben. Ein Autoklav ist optional und nur dann erforderlich, wenn Sie Ihre eigenen Medien sterilisieren oder Abfälle entsorgen möchten. Möglicherweise benötigen Sie auch einen separaten Raum für die Anreicherung und die Tests. Bei der Verwendung von Lateral-Flow-Streifen ist keine zusätzliche Ausrüstung für die Auswertung der Ergebnisse erforderlich, so dass keine größeren Investitionen notwendig sind.
Mythos 3
Tests auf Krankheitserreger erfordern gut geschultes Personal
Die Schnellmethoden für Krankheitserreger wurden im Vergleich zu den Tagen, an denen nur hochqualifizierte Mikrobiologen solche Tests durchführen konnten, rationalisiert, zusammen mit unzähligen Röhrchen, Platten und einem scharfen Auge. Je nach Methode sind immer noch verschiedene Fähigkeiten erforderlich, aber viele Testkits können von geschultem Personal effektiv durchgeführt werden. Nicht alle Testmethoden erfordern hochqualifiziertes Personal. In vielen Unternehmen kann es sein, dass das Laborpersonal aus dem Produktionsbetrieb übernommen wurde und keinen wissenschaftlichen Abschluss hat. Die Testmethoden sollten daher einfach und robust sein und nur wenige Schritte umfassen, um die Arbeitsabläufe im Labor zu rationalisieren und das Risiko von Fehlern zu minimieren. Ein Labor muss auch nachweisen können, dass seine Mitarbeiter in der jeweiligen Testmethode geschult wurden. Einige Unternehmen nehmen auch an Eignungstestprogrammen teil, um sicherzustellen, dass ihre Labormitarbeiter unabhängig arbeiten können, um genaue Testergebnisse zu erzielen.
Mythos 4
Die Anforderungen an die Laborsicherheit halten kleine Unternehmen davon ab, ihre eigenen Tests durchzuführen
Lebensmittelpathogene der so genannten Risikogruppe 2, wie Salmonellen, Listerien und E.coli O157, können mit einigen geringfügigen Anpassungen in Räumen behandelt werden. Krankheitserreger dieser Risikogruppe gelten nicht als gefährlich für das Laborpersonal und die Bevölkerung im Allgemeinen. Gemäß der EN 12128 (Europäische Norm), Biosicherheit in mikrobiologischen und biomedizinischen Laboratorien (US Centers for Disease Control and Prevention) und dem Biosicherheitshandbuch der Weltgesundheitsorganisation (WHO) sollten solche Räume mit dem Symbol für biologische Gefahren gekennzeichnet und der Zugang beschränkt sein. Nur diejenigen, die mit den Krankheitserregern arbeiten, sollten Zugang zu diesem Laborraum haben. Die Oberflächen in diesem Raum müssen gegen Chemikalien und damit auch gegen Desinfektionsmittel beständig sein. Diese Anforderungen an die Laborsicherheit können von kleinen Lebensmittelherstellern leicht erfüllt werden.
Mythos 5
Ich kann kontaminiertes Testmaterial nicht entsorgen
Doch, das können Sie. Hier sind drei Möglichkeiten für eine sichere Entsorgung: 1. Verwenden Sie einen Autoklaven und stellen Sie die Temperatur auf 121°C für mindestens 20 Minuten ein. Das Material kann nun sicher als Restmüll entsorgt werden. 2. Verwenden Sie ein Mikrowellen-Desinfektionssystem. Das Material kann nun sicher als Restmüll entsorgt werden. 3. Beauftragen Sie ein Abfallunternehmen mit dieser Aufgabe. Diese wird spezielle Container bestellen, um den kontaminierten Abfall zu sammeln und für Sie zu entsorgen.
Veröffentlicht am:
Mikrobiologie
Dieser Artikel wurde in Spot On #3 veröffentlicht.
Sind Sie neugierig, was Spot On zu bieten hat?
Jetzt lesen
Mythos 6
Nach einem positiven Testergebnis müssen die Proben nicht weiter analysiert werden
Alle im Handel erhältlichen Schnellmethoden sind Screening-Tests und erfordern nach einem "mutmaßlich positiven" Testergebnis eine kulturelle Bestätigung. Zur Bestätigung muss die angereicherte Testportion auf Selektivagar gestreut werden, um eine typische Kolonie auf der Grundlage morphologischer und biochemischer Merkmale zu isolieren. Dies gilt insbesondere für die Untersuchung von Endprodukten oder Lebensmitteln. Bei Umweltproben wird eine kulturelle Bestätigung nur selten durchgeführt, da häufig zusätzliche Hygienemaßnahmen ergriffen werden. Es gibt mehrere Optionen für Selektivagarplatten, wobei die gängigsten im USDA Microbiology Laboratory Guidebook (MLG), im FDA Bacteriological Analytical Manual (BAM) oder in den ISO-Referenzhandbüchern zu finden sind (siehe Tabelle 1).

Mythos 7
Es gibt keinen Grund, auf Listeria-Spezies zu testen, wenn L. monocytogenes der Verunreiniger ist
Listeria monocytogenes (L'mono) mag der einzige regulierte Listeria-Stamm sein, aber er ist nicht der einzige pathogene. Listeria ivanovii ist ein weiterer pathogener Stamm, der in Ihrer Einrichtung vorkommen kann. Ein weiterer Grund für die Untersuchung von Listeria spp. (alle Listeria-Stämme), insbesondere in der Verarbeitungsumgebung, besteht darin, Wachstumsnischen aufzuspüren. Denn L'mono kann möglicherweise dort wachsen, wo andere Listeria-Stämme gedeihen. Es ist eine Frage der Wahrscheinlichkeit, ob L'mono vorhanden ist oder nicht. Wenn viele nicht-pathogene Listeria-Stämme (wie z.B. Listeria innocua) in einer Probe vorhanden sind, könnten sie L'mono im Anreicherungsprozess "überwuchern" und möglicherweise ein falsch-negatives Ergebnis verursachen. Es ist nicht möglich, während der selektiven Anreicherung nur eine Listeria-Spezies (d.h. L'mono) anzubauen.
Mythos 8
Alle im Handel erhältlichen Methoden sind gleich
Es gibt heute eine Vielzahl von Schnellmethoden auf dem Markt, und die Wahl zwischen ihnen kann entmutigend sein. Wie kann ein Lebensmittelhersteller entscheiden, welche Methode für ihn die beste ist? Alle im Handel erhältlichen Schnellmethoden bestehen aus zwei Teilen - einer Anreicherung, gefolgt von einem Nachweisschritt. Während der Anreicherungsphase werden unterschiedliche Medien verwendet, entweder eine herkömmliche oder eine eigene Brühe. Der Hauptunterschied liegt in der Nachweisphase. Immunoassay-Methoden weisen Proteine nach, während PCR-Methoden DNA nachweisen. Die folgenden Bewertungskriterien sollten berücksichtigt werden: Einschlussfähigkeit, Ausschlussfähigkeit, Empfindlichkeit, Spezifität, Nachweisgrenze, Reproduzierbarkeit, Wiederholbarkeit und Zertifizierung (siehe Tabelle 2).
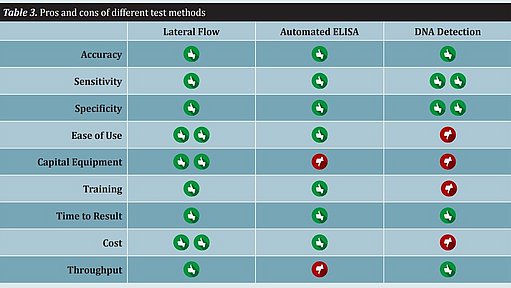
Schnellmethoden unterscheiden sich erheblich in Bezug auf Arbeitsablauf, Benutzerfreundlichkeit und Durchsatz. Zu den weiteren Merkmalen einer Testmethode, die berücksichtigt werden sollten, gehören der Aufwand für die Ausrüstung, die Schulung, die Zeit bis zum Ergebnis und die Kosten. All diese Eigenschaften müssen bei der Einführung einer Schnellmethode berücksichtigt werden. Es gibt keine einzige Methode, die für alle Lebensmittelhersteller geeignet ist (siehe Tabelle 3).