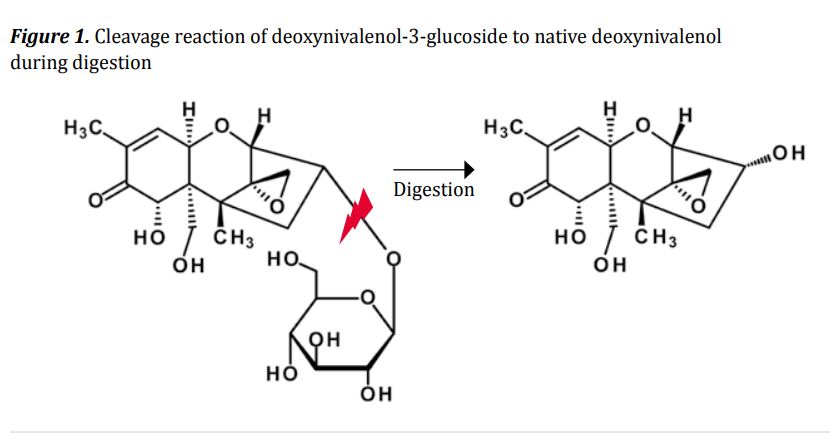
Neu auftretende Mykotoxine - eine Bedrohung jenseits von Vorschriften?

Mykotoxine sind natürlich vorkommende, sekundäre Stoffwechselprodukte, die von verschiedenen Schimmelpilzen produziert werden. Diese Verbindungen sind für Menschen und Tiere giftig. Toxigene Schimmelpilze kontaminieren eine Vielzahl von Nutzpflanzen und produzieren Mykotoxine als Folge der Infektion von Pflanzengewebe auf dem Feld. Leider kann sich die Bildung dieser Toxine auch nach der Ernte fortsetzen, und der Gehalt an Mykotoxinen in Getreide steigt während der Lagerung weiter an. Kontaminierte Feldfrüchte stellen ein großes Gesundheitsrisiko für Mensch und Tier dar. Die bekanntesten Mykotoxin-produzierenden Feldpilze sind die Pilze der Arten Fusarium und Aspergillus. Darüber hinaus gibt es über 300 verschiedene Pilze, von denen bekannt ist, dass sie über 400 verschiedene Mykotoxine produzieren. In den letzten Jahren wurden immer mehr Mykotoxine als relevant eingestuft, da sie zu den Risiken für Mensch und Tier beitragen. Studien zur Risikobewertung wurden für verschiedene wichtige Mykotoxingruppen durchgeführt, darunter Mutterkornalkaloide (siehe Artikel über Mutterkornalkaloide), Alternaria-Toxine (siehe Artikel über Alternaria-Toxine) und modifizierte oder maskierte Mykotoxine.
Modifizierte Mykotoxine als Pflanzenschutzmittel
Mykotoxine werden in der Regel explizit von Pilzen produziert und ihre Ausgangsstruktur wird häufig vom Pilz selbst modifiziert, der einen Cocktail strukturell verwandter Verbindungen freisetzt. Während der Infektion werden diese Substanzen dann oft von der Wirtspflanze des Pilzes weiter modifiziert. Die lebende Pflanze kann die chemische Struktur der Toxine verändern und so genannte maskierte Mykotoxine produzieren. Die Bildung dieser maskierten Toxine ist eine wichtige Entgiftungsstrategie von Nutzpflanzen, da sie für die Pflanze weniger giftig sind. In der Regel ist ein Glukosemolekül oder ein Sulfat an der Konjugation und Entgiftung beteiligt. Obwohl diese maskierten Toxine die Pflanze nicht weiter schädigen, kann ihre Toxizität für Menschen und Tiere wieder auftauchen, wenn das hinzugefügte Maskierungsmolekül bei der Verdauung im Magen-Darm-Trakt von Säugetieren gespalten wird (Abbildung 1). In der Pflanzenzucht könnte das zunehmende Auftreten und die Produktion einiger maskierter Mykotoxine mit neuartigen resistenten Rassen zusammenhängen. Deoxynivalenol-3-glucosid zum Beispiel wurde Berichten zufolge mit der Resistenz gegen die Kraut- und Knollenfäule (Fusarium) in Verbindung gebracht. Das bedeutet, dass Fusarium-resistente Pflanzen nachweislich ein höheres Verhältnis von Deoxynivalenol-3-glucosid zu Deoxynivalenol aufweisen, dass aber gleichzeitig der Gesamtgehalt an Deoxynivalenol und der modifizierten Form aufgrund der höheren Fusarium-Resistenz geringer ist.
Der Begriff "modifiziertes Mykotoxin" umfasst sowohl die Modifizierung eines Elterntoxinmoleküls durch den Pilz selbst als auch die Maskierung des Toxins, die nur im Pflanzengewebe stattfindet. Eine andere Art der Modifikation findet bei Säugetieren statt, wenn Aflatoxin B1 durch kontaminiertes Futter aufgenommen und in Aflatoxin M1 umgewandelt wird. Dieses Aflatoxin M1 wandert in die Milch säugender Tiere und wird mit ihr ausgeschieden. Darüber hinaus können die Toxine auch bei der Verarbeitung von Lebensmitteln, insbesondere beim Erhitzen und bei der Fermentation, verändert werden, was ihre Prävalenz erhöht. Diese modifizierten Mykotoxine können in relevanten Mengen in Lebens- und Futtermitteln vorkommen. Das Phänomen der modifizierten Mykotoxine betrifft insbesondere Fusarientoxine (Trichothecene, Zearalenon und Fumonisine), aber auch für andere Mykotoxine wie Aflatoxine, Ochratoxin A oder Patulin wurden modifizierte Formen gemeldet.
Veränderte und maskierte Formen von Deoxynivalenol - ein Beispiel
Deoxynivalenol ist das Mykotoxin mit den meisten Studien, die zu den verschiedenen Versionen der häufig beobachteten Veränderungen durchgeführt wurden. Die modifizierten Formen von Deoxynivalenol lassen sich in zwei Hauptgruppen unterteilen: veränderte und maskierte Formen. Es gibt zwei wichtige veränderte Formen von Deoxynivalenol, die vom Pilz selbst ausgeschieden werden: 3-Acetyl-Deoxynivalenol und 15-Acetyl-Deoxynivalenol, wie es in Fusarium-verseuchtem Getreide vorkommt. Pflanzen sind in der Lage, das Deoxynivalenol zu Deoxynivalenol-3-Glucosid zu maskieren, das, wie neuere Studien zeigen, zwei sulfonierte Formen annehmen kann: Deoxynivalenol-3-Sulfat und Deoxynivalenol-15-Sulfat (Tabelle 1).
Wie schädlich sind modifizierte und neu auftretende Mykotoxine?
Modifizierte Mykotoxine können entweder mehr oder weniger giftig sein als ihre Ausgangsstoffe. Zum Beispiel können sie aufgrund von Modifikationen besser bioverfügbar sein. Es gibt nur wenige toxikologische Daten über modifizierte Mykotoxine, und die aktuellen Ergebnisse und Kenntnisse über die tatsächlichen Risiken und Auswirkungen dieser Verbindungen sind unzureichend. Dieser Mangel an Wissen macht es schwierig, eine angemessene Risikobewertung durchzuführen. Dennoch gibt es Studien, die ihre potenzielle Bedrohung für die Lebensmittelsicherheit beschreiben. Darüber hinaus ist hervorzuheben, dass maskierte Mykotoxine im Verdauungstrakt von Tieren und Menschen wieder "demaskiert" werden können, wodurch die Ausgangsverbindung mit ihren toxikologischen Wirkungen wieder freigesetzt wird. Ähnlich verhält es sich mit neu auftretenden Mykotoxinen: Es liegen nur wenige toxikologische Daten vor, was die Festlegung von Vorschriften und Höchstwerten zum Schutz von Mensch und Tier vor möglichen Gesundheitsrisiken erschwert.
Decken die Vorschriften alle Mykotoxin-Risiken ab?
Um die Sicherheit von Lebens- und Futtermitteln zu gewährleisten, haben viele Länder gesetzliche Grenzwerte für Mykotoxine in Nutzpflanzen festgelegt. Derzeit gibt es in den meisten Industrieländern Vorschriften über Höchstwerte oder zumindest Richtwerte für Mykotoxine in Lebens- und Futtermitteln. Diese Vorschriften gelten nur für einige der bekannten Mykotoxine wie Aflatoxine B1, B2, G1, G2 und M1; Fumonisine B1, B2 und B3; Ochratoxin A, Deoxynivalenol, Zearalenon, HT-2-Toxin und T-2-Toxin. Da sich modifizierte Mykotoxine in ihren chemischen Reaktionen anders verhalten als die ursprünglichen Mykotoxine, können sie bei Routineanalysen leicht übersehen werden. Die derzeitigen Nachweismethoden für regulierte Mykotoxine in Lebens- und Futtermitteln beinhalten kein Routine-Screening auf diese modifizierten Mykotoxine, da sie nicht von der Gesetzgebung abgedeckt sind. Solche Standardmethoden können Kontaminationen unterhalb der gesetzlichen Grenzwerte aufzeigen, während Kontaminationen durch modifizierte Mykotoxine unentdeckt bleiben. Dies ist ein richtiges Ergebnis, aber aus toxikologischer Sicht würde die Einbeziehung modifizierter Toxine (z.B. als Summenparameter) fundiertere Daten für die Risikobewertung liefern. All diese Fakten zusammengenommen weisen auf die möglichen Gefahren hin, die von modifizierten Mykotoxinen für die menschliche Gesundheit ausgehen. In der Europäischen Union werden derzeit Verordnungen über Höchstwerte für modifizierte Mykotoxine sowie für andere neu auftretende Mykotoxine diskutiert.
Analysemethoden für die Quantifizierung von Mykotoxinen
Mykotoxine werden in der Regel mit chromatographischen Methoden wie der Flüssigchromatographie-Massenspektrometrie (LC-MS) und immunchemischen Methoden wie dem enzymatischen Immunoassay (ELISA) analysiert. Immunchemische Methoden können, abhängig von der Kreuzreaktivität des Antikörpers, auf mehr als eine Verbindung (z.B. native Mykotoxine und ihre modifizierten Formen) reagieren und zu einem einzigen Ergebnis führen. Im Gegensatz dazu können LC-basierte Trennmethoden die Gesamtmenge der Toxine unterschätzen, da diese Methoden jede Verbindung als einen einzelnen Parameter auflösen und in der Regel nur für die Muttermykotoxine entwickelt werden.
Grenzen der Analysemethoden
Es gibt zwei Möglichkeiten, modifizierte Mykotoxine nachzuweisen und zu quantifizieren: Ein "direkter" Ansatz, bei dem die gesamte modifizierte Verbindung gemessen wird, und ein "indirekter" Ansatz, bei dem die Ausgangsverbindung nach chemischen oder enzymatischen Behandlungen gemessen wird, die zur Spaltung der modifizierten Mykotoxine führen, hauptsächlich durch Hydrolyse. Zu den Vorteilen der indirekten Methode gehört, dass für eine korrekte Quantifizierung keine Referenzmaterialien für modifizierte Mykotoxine benötigt werden und dass alle modifizierten Formen im Endergebnis enthalten sind. Die Hauptnachteile sind, dass die Effizienz des Hydrolyseprozesses nicht einfach überprüft werden kann und dass es keinen Zugang zu den Mengen der verschiedenen Formen eines Toxins gibt. Daher ist es wichtig, direkte Methoden zu entwickeln, um weitere Erkenntnisse über das Vorkommen modifizierter Mykotoxine zu gewinnen. Alle chromatographischen Technologien für die Stamm-Mykotoxine sind potenziell auch für ihre modifizierten Formen geeignet, solange sie löslich und direkt für die Analyse verfügbar sind. Eine große Einschränkung bei der direkten Bestimmung und Quantifizierung modifizierter Mykotoxine ist die begrenzte Verfügbarkeit von Referenzmaterialien (Reinsubstanzen oder Kalibriermittel zusätzlich zu isotopenmarkierten internen Standards). Ein weiterer Nachteil ist, dass die meisten Methoden eine angemessene Reinigung vor dem Analyseverfahren erfordern. Kommerziell erhältliche Reinigungsgeräte sind derzeit für native Mykotoxine konzipiert und eignen sich nicht unbedingt für modifizierte Formen. Derzeit wird an der Entwicklung neuer Referenzstandards sowie innovativer Reinigungsgeräte gearbeitet, um modifizierte Mykotoxine direkt zu bestimmen.
Neu auftretende Mykotoxine - eine Bedrohung jenseits der Vorschriften?
Angesichts der derzeitigen Lücken in der routinemäßigen Mykotoxinanalyse, die auf fehlende Vorschriften für neu auftretende Mykotoxine zurückzuführen sind, können viele dieser Verbindungen unentdeckt bleiben und eine Gefahr für die Gesundheit von Mensch und Tier darstellen. Das Ausmaß dieser Bedrohung, das als beträchtlich angesehen wird, ist jedoch schwer abzuschätzen, da es trotz zunehmender Forschungsanstrengungen in dieser Richtung nur wenige toxikologische Daten gibt.
Veröffentlicht am:
Mykotoxin
Dieser Artikel wurde in Spot On #5 veröffentlicht.
Sind Sie neugierig, was Spot On zu bieten hat?
Magazin aufrufen